Arbeitsblatt: chemie
Material-Details
chemie
Chemie
Reaktionsgleichungen
9. Schuljahr
2 Seiten
Statistik
121382
2056
8
22.09.2013
Autor/in
mafe d gregorio
Land: Schweiz
Registriert vor 2006
Textauszüge aus dem Inhalt:
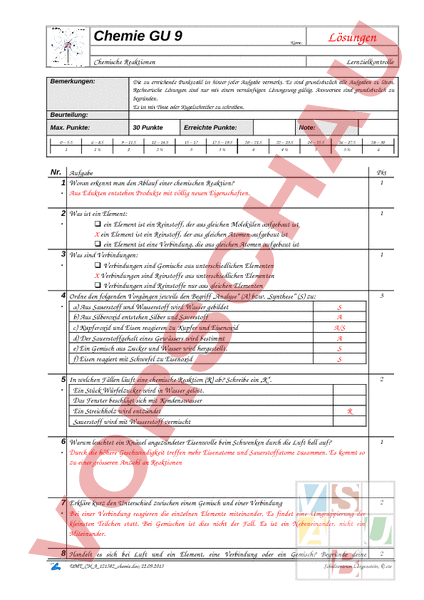
Chemie GU 9 Lösungen Name: Chemische Reaktionen Lernzielkontrolle Die zu erreichende Punktzahl ist hinter jeder Aufgabe vermerkt. Es sind grundsätzlich alle Aufgaben zu lösen. Rechnerische Lösungen sind nur mit einem vernünftigen Lösungsweg gültig. Antworten sind grundsätzlich zu begründen. Es ist mit Tinte oder Kugelschreiber zu schreiben. Bemerkungen: Beurteilung: Max. Punkte: 30 Punkte Erreichte Punkte: Note: 0 – 5.5 6 – 8.5 9 – 11.5 12 – 14.5 15 – 17 17.5 – 19.5 20 – 21.5 22 – 23.5 24 – 25.5 26 – 27.5 28 – 30 1 1 2 2 3 3 4 4 5 5 6 Pkt 1 Nr. Aufgabe 1 Woran erkennt man den Ablauf einer chemischen Reaktion? Aus Edukten entstehen Produkte mit völlig neuen Eigenschaften. 2 Was ist ein Element: ein Element ist ein Reinstoff, der aus gleichen Molekülen aufgebaut ist 1 3 1 4 ein Element ist ein Reinstoff, der aus gleichen Atomen aufgebaut ist ein Element ist eine Verbindung, die aus gleichen Atomen aufgebaut ist Was sind Verbindungen: Verbindungen sind Gemische aus unterschiedlichen Elementen Verbindungen sind Reinstoffe aus unterschiedlichen Elementen Verbindungen sind Reinstoffe nur aus gleichen Elementen Ordne den folgenden Vorgängen jeweils den Begriff „Analyse (A) bzw. „Synthese (S) zu: a) Aus Sauerstoff und Wasserstoff wird Wasser gebildet b) Aus Silberoxid entstehen Silber und Sauerstoff c) Kupferoxid und Eisen reagieren zu Kupfer und Eisenoxid d) Der Sauerstoffgehalt eines Gewässers wird bestimmt e) Ein Gemisch aus Zucker und Wasser wird hergestellt. f) Eisen reagiert mit Schwefel zu Eisenoxid 5 In welchen Fällen läuft eine chemische Reaktion (R) ab? Schreibe ein „R. Ein Stück Würfelzucker wird in Wasser gelöst. Das Fenster beschlägt sich mit Kondenswasser Ein Streichholz wird entzündet Sauerstoff wird mit Wasserstoff vermischt 3 A A/S S 2 6 Warum leuchtet ein Knäuel angezündeter Eisenwolle beim Schwenken durch die Luft hell auf? Durch die höhere Geschwindigkeit treffen mehr Eisenatome und Sauerstoffatome zusammen. Es kommt so zu einer grösseren Anzahl an Reaktionen 1 7 Erkläre kurz den Unterschied zwischen einem Gemisch und einer Verbindung Bei einer Verbindung reagieren die einzelnen Elemente miteinander. Es findet eine Umgruppierung der kleinsten Teilchen statt. Bei Gemischen ist dies nicht der Fall. Es ist ein Nebeneinander, nicht ein Miteinander. 2 8 Handelt es sich bei Luft und ein Element, eine Verbindung oder ein Gemisch? Begründe deine 2 UMT_CH_9_121382_chemie.doc; 22.09.2013 Schulzentrum Längenstein, ste Chemie GU 9 Lernzielkontrolle Entscheidung. Luft ist ein Gemisch aus Stickstoff, Sauerstoff, Kohlendioxid und andern Gasen. 9 Zeichne den Reaktionsverlauf einer exothermen Reaktion und trage die folgenden Begriffe richtig in die Grafik ein: Edukte, Produkte, Wo erkennt man die Aktivierungsenergie? Wo kann die Reaktionsenthalpie herausgelesen werden? 4 1 Obwohl Magnesium sehr heftig mit Sauerstoff reagieren kann, muss ein Magnesiumband zunächst stark 0 erhitzt werden, bis es mit Sauerstoff reagiert. Warum? Handelt es sich bei der Bildung von Magnesiumoxid aus den Elementen um eine exotherme oder endotherme Reaktion? Mit der Flamme muss zunächst eine gewisse Aktivierungsenergie zugeführt werden. Danach läuft die Reaktion von alleine ab, also exotherm 2 1 Wird ein Gemisch aus 4g Schwefel und 8g Zinkpulver mit einer glühenden Nadel berührt, so tritt eine sehr 1 heftige Reaktion ein. Zurück bleibt ein bei hoher Temperatur gelber und nach dem Abkühlen weisser Stoff. a) Welcher Stoff ist wohl entstanden? Formuliere das Reaktionsschema Zink Schwefel Zinksulfid. b) Verläuft die Reaktion exotherm oder endotherm? Begründe exotherm c) Warum genügt es, das Gemisch nur an einer Stelle zu erhitzen? Die Aktivierungsenergie reicht aus, um eine Reaktion ablaufen zu lassen. Dort wird soviel Energie freigesetzt, um benachbarte Atome anzuregen und auch reagieren zu lassen. 4 1 In eine wassergefüllte Wanne wird eine Glasglocke gestellt. Auf einem Verbrennungslöffel, der in einem 2 durchbohrten Stopfen steckt, wird eine kleine Portion des Nichtmetalls Phosphor entzündet und die Glasglocke wird geschlossen. Der Phosphor verbrennt zu einem weissen Feststoff. Obwohl noch genügend Phosphor vorhanden ist, hört der Verbrennungsvorgang auf. Der Wasserspiegel steigt in der Glasglocke nach kurzer Zeit an. a) Um welchen Stoff kann es sich bei dem weissen Feststoff handeln? b) Warum hört die Reaktion plötzlich auf? c) Warum steigt das Wasser in der Glasglocke an? d*) Um wie viel steigt der Wasserspiegel prozentual an? 3 UMT_CH_9_121382_chemie.doc; 22.09.2013 Schulzentrum Längenstein, ste Chemie GU 9 Lernzielkontrolle a) Beim weissen Pulver handelt es sich um Phosphoroxid. Beim Verbrennen verbindet sich der Phosphor mit dem Sauerstoff. b) Die Reaktion hört auf, weil es keinen Sauerstoff mehr gibt in der Umgebung c) Da der Sauerstoff weg ist, reduziert sich das Volumen der Luft d) Das Volumen wird um 1/5 reduziert. (21% Sauerstoffanteil in der Luft) UMT_CH_9_121382_chemie.doc; 22.09.2013 Schulzentrum Längenstein, ste Chemie GU 9 Lernzielkontrolle 1 Erhitzt man orangefarbenes Quecksilberoxid im Reagenzglas, wird die Stoffportion langsam kleiner. An den 3 kälteren Teilen des Glases setzen sich silbrig glänzende Tröpfchen ab. Gleichzeitig kann man ein Gas über Wasser als Sperrflüssigkeit auffangen. Hält man einen glimmenden Holzspan in das mit dem Gas gefüllte Reagenzglas, so flammt er hell auf und verbrennt mit heller Flamme. a) Deute die Versuchsbeobachtung b) Formuliere das Reaktionsschema c) Verläuft die Reaktion exotherm oder endotherm? Begründe d) Warum darf der Reagenzglasinhalt nicht in den Ausguss geschüttet werden? 4 a) Das unbekannte Gas müsste eigentlich Sauerstoff sein. b) HgO Hg O c) endotherm d) Quecksilber ist ein Schwermetall und darf nicht in Abwässer gelangen. UMT_CH_9_121382_chemie.doc; 22.09.2013 Schulzentrum Längenstein, ste