Arbeitsblatt: chemische Begriffe
Material-Details
Definition chemischer Begriffe
Chemie
Anderes Thema
7. Schuljahr
2 Seiten
Statistik
173728
846
0
19.08.2017
Autor/in
Adolf Adolf Kuster
Land: Schweiz
Registriert vor 2006
Textauszüge aus dem Inhalt:
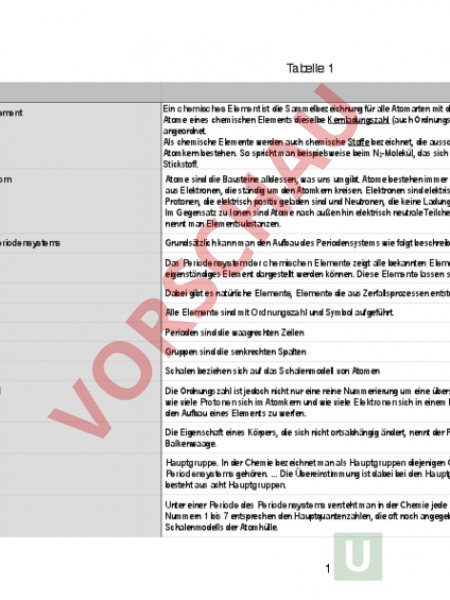
Tabelle 1 Was ist ein Element Was ist ein Atom Aufbau des Periodensystems Ein chemisches Element ist die Sammelbezeichnung für alle Atomarten mit derselben Anzahl an Protonen im Atomkern. Somit haben alle Atome eines chemischen Elements dieselbe Kernladungszahl (auch Ordnungszahl). Sie werden im Periodensystem der Elemente angeordnet. Als chemische Elemente werden auch chemische Stoffe bezeichnet, die ausschließlich aus Atomen mit gleicher Anzahl an Protonen im Atomkern bestehen. So spricht man beispielsweise beim N2-Molekül, das sich aus zwei Stickstoffatomen zusammensetzt, von elementarem Stickstoff. Atome sind die Bausteine alldessen, was uns umgibt. Atome bestehen immer aus einem Atomkern und einer Atomhülle. Die Hülle besteht aus Elektronen, die ständig um den Atomkern kreisen. Elektronen sind elektrisch negativ geladen. Der Kern wiederum besteht aus Protonen, die elektrisch positiv geladen sind und Neutronen, die keine Ladung besitzen.Jedes Element hat eine ihm eigene Art von Atomen. Im Gegensatz zu Ionen sind Atome nach außen hin elektrisch neutrale Teilchen. Stoffe, die nur aus Atomen der gleichen Art aufgebaut sind, nennt man Elementsubstanzen. Grundsätzlich kann man den Aufbau des Periodensystems wie folgt beschreiben: Das Periodensystem der chemischen Elemente zeigt alle bekannten Elemente, aus der die Erdkruste besteht und die als eigenständiges Element dargestellt werden können. Diese Elemente lassen sich nicht chemisch in weitere Stoffe zerlegen. Dabei gibt es natürliche Elemente, Elemente die aus Zerfallsprozessen entstehen und Elemente die künstlich hergestellt werden. Alle Elemente sind mit Ordnungszahl und Symbol aufgeführt. Perioden sind die waagrechten Zeilen Gruppen sind die senkrechten Spalten Schalen beziehen sich auf das Schalenmodell von Atomen Ordnungszahl Die Ordnungszahl ist jedoch nicht nur eine reine Nummerierung um eine übersichtliche Anordnung zu ermöglichen. Sie gibt außerdem an, wie viele Protonen sich im Atomkern und wie viele Elektronen sich in einem Element befinden. Hier lohnt es sich, einen kurzen Blick auf den Aufbau eines Elements zu werfen. Masse Die Eigenschaft eines Körpers, die sich nicht ortsabhängig ändert, nennt der Physiker seine Masse. Masse bestimmt man mit einer Balkenwaage. Hauptgruppe Hauptgruppe. In der Chemie bezeichnet man als Hauptgruppen diejenigen Gruppen des Periodensystems, die zum s- und p-Block des Periodensystems gehören. . Die Übereinstimmung ist dabei bei den Hauptgruppen am größten. Das Periodensystem der Elemente besteht aus acht Hauptgruppen. Periode Unter einer Periode des Periodensystems versteht man in der Chemie jede Zeile des Periodensystems der Elemente. Die PeriodenNummern 1 bis 7 entsprechen den Hauptquantenzahlen, die oft noch angegebenen Perioden-Buchstaben bis den Schalen des Schalenmodells der Atomhülle. 1 Stoffumwandlung Chemische Reaktionen sind Vorgänge, bei denen aus den Ausgangsstoffen neue Stoffe, Reaktionsprodukte, mit neuen Eigenschaften entstehen. Es erfolgt eine Stoffumwandlung, die immer mit einer Energieumwandlungen verbunden ist. Reaktionsschema Ein Reaktionsschema ist in der Chemie die symbolische Wiedergabe einer Stoffumwandlung (chemische Reaktion) in Form von Formeln und stöchiometrischen Koeffizienten sowie einem Reaktionspfeil (). Es wird auch Reaktionsgleichung oder chemische Gleichung genannt Oxidation Die Oxidation ist eine chemische Reaktion, bei der ein Atom, Ion oder Molekül Elektronen abgibt. Seine Oxidationszahl wird dabei erhöht.[1] Ein anderer Stoff nimmt die Elektronen auf und wird reduziert. Beide Reaktionen zusammen werden als Teilreaktionen einer Redoxreaktion betrachtet. Synthese Als Synthese bezeichnet man den Umsatz (die Vereinigung) von zwei oder mehr Elementen (Bestandteilen) zu einer neuen Einheit. Analyse Die Zerlegung einer chemischen Verbindung nennt man Analyse. Elektrolyse Einen Prozess, bei dem ein elektrischer Strom eine Redoxreaktion erzwingt, nennt man Elektrolyse. Sie wird beispielsweise zur Gewinnung von Metallen verwendet, oder zur Herstellung von Stoffen, deren Gewinnung durch rein chemische Prozesse teurer oder kaum möglich wäre. endotherm Eine endotherme Reaktion ist eine chemische Reaktion, bei der Energie aus der Umgebung aufgenommen wird. exotherm Bei der exothermen Reaktion wird Wärmeenergie an die Umgebung abgegeben. Molekül Moleküle bestehen aus zwei oder mehr miteinander verbundenen Atomen. Wertigkeit Die Wertigkeit, auch Valenz, eines Atoms eines chemischen Elements gibt an, wie viele Atome es im Falle einer chemischen Bindung an sich binden kann, bzw. wie viele Einfachbindungen es mit anderen Atomen eingehen müsste, um den Oktettzustand zu erreichen. Sie dient somit der Berechnung von chemischen Formeln (Summenformeln) einfacher chemischer Verbindungen. Summenformel Die Summenformel gibt ausschließlich die mengenmäßige Zusammensetzung der an dem Molekül einer Verbindung beteiligten Atome an. Strukturformel Mit der Strukturformel einer Verbindung wird die räumliche Anordnung der an der Verbindung beteiligten Atome angegeben. Molekülmodell Das Stäbchenmodell, auch Gittermodell genannt, ist eine dreidimensionale Darstellungsart einer Molekülstruktur, deren (kovalente) Atombindungen in Stabform dargestellt werden. Für rein ionische Verbindungen gibt es das analoge Gittermodell. Darstellungsmäßig abgegrenzt sind hiervon das Strichmodell (dünne Linien), das Kugel-Stab-Modell und das Kalottenmodell. Für große Proteine gibt es das Bändermodell. 2